
核磁共振成像(magnetic resonance imaging, MRI)是临床上重要的影像学诊断检查技术,具有高空间清晰度与分辨率、无射线辐射和不需注射碘对比剂等特点,在软组织、骨关节和心脏成像方面具有其它影像技术不可比拟的优势[1],但却不能用于检查安置心脏电子植入装置(cardiac implantable electrical device, CIED)的患者。据统计,美国大约有2000000人装有CIED,其中50%~75%具有MRI检查指征[2]。近20年,人们在不断探索解决这一矛盾的途径,从个例探索到小规模研究[3-5],再到技术革新,总体结论是CIED患者进行MRI检查的获益大于风险[2]。2007年,AHA声明明确指出,几乎所有置入冠状动脉支架和人工心脏瓣膜与瓣环患者进行3.0 T(Tesla,特斯拉,磁场强度单位)以下MRI检查都是安全的[6];但起搏器功能却仍可能受电磁效应的干扰,甚至损坏。2008年,第一台MRI兼容性起搏器上市,使CIED患者MRI检查的安全性得到进一步保障,本文将就近年来该领域的进展做一综述。特别说明,本文中CIED限定为心脏起搏器和植入式心脏复律除颤器(implantable cardiac defibrillator, ICD)。
1 从基本原理看MRI对CIED的作用环节
MRI装置主要由磁体、谱仪和图像处理系统三部分构成。人体组织的氢原子核具有自旋特性,在通常情况下,其自旋轴呈任意取向而无规律,因而磁矩相互抵消,净磁矩为零。在MRI检查时,静磁场使氢原子核磁矩按磁力线方向排列,形成纵向净磁矩(也称宏观磁化向量,即单位体积中全部原子核的磁矩,图1A)[7]。当射频发生器向人体组织发射高频脉冲时,氢核即可产生共振效应,净磁矩横向偏转,并处于激活旋转状态,停止发放脉冲后,氢核将随即恢复至静磁场下的纵向排列状态(这一过程称为弛豫过程,relaxation,图1B),同时释放电信号。快速切换的梯度磁场以线性方式沿梯度线圈轴改变纵向磁矩,引起氢原子核Larmor频率的微小改变,这样就可以识别氢原子核在三维空间中的位置,从而对MR信号进行空间编码[7](图1C)。经图像处理系统对电信号进行分析即可获得MRI图像[8]。因此,在MRI检查时会同时存在静磁场、梯度磁场和射频磁场三种磁场(图1),其中临床使用的静磁场强度为0.5~5 T,相当于地球磁场的104~105倍。而CIED中均含铁磁性金属元件,会与空间磁场相互作用,产生作用力、感应电流和电磁干扰等物理效应,可能损害、改变或干扰CIED本身或功能参数,以致造成一系列临床不良事件,这便是禁止CIED患者MRI检查的理论基础。
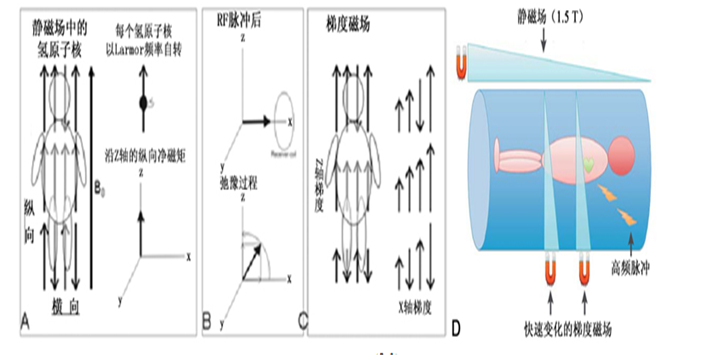
图1 MRI的成像原理和系统中可能影响CIED的3种成份[7, 9]:A.静磁场使人体中氢核沿Z轴纵向排列;B.射频(RF)脉冲使氢核共振,净磁矩横向偏转,脉冲停止后氢核重新纵向排列并释放电信号;C.沿Z轴和X轴施加快速变化的梯度磁场,以获取氢核的空间位置;D.3种磁场的宏观示意图。
2 MRI与CIED的相互作用
2.1 磁力和磁矩效应:在MRI检查时,静磁场对CIED中的铁磁性元件(ferromagnetic components)等金属材料,如铁、钴、镍及其合金会产生磁力和磁矩,可能造成脉冲发生器和电极导线移位。研究显示,MRI对起搏器可产生0.05~3.6 N的作用力,对ICD可产生1.0~5.9 N的作用力[10]。通常,当作用力在2 N以下时,CIED系统不会产生移位效应;而作用力的大小则与铁磁性元件含量和磁场强度正相关。因此,限制铁磁性金属含量和MRI场强是减少机械作用力的有效途径。截至目前,针对CIED人群进行的MRI研究大多采用1.5 T以下(包括1.5 T)的静磁场强度,尚未发现因器械移位而引起的不良事件[3-5]。
2.2 起搏模式自动转换:在按需型起搏器中,MRI中的静磁场能够作用于磁簧片开关,产生不可预知的簧片开关功能转换,即起搏模式在同步和非同步之间转换[11]。当自主心率大于起搏频率时,在非同步模式下起搏可能引起竞争心律。
2.3 电极导线的热效应:在MRI检查时,具有导电性的电极导线可作为一根天线,可能会接收MRI产生的射频能量,射频磁场可使电极导线系统产生感应电流,进一步沿电极导线传至心肌组织并转换成热能,造成心脏组织的热损伤,使周围心肌水肿和瘢痕形成。临床上最常见的后果是起搏阈值增加,进而造成起搏失效,严重时还可引起心脏穿孔。Martin等[5]报道了54名非起搏依赖患者经历62次非限制MRI检查的结果,大约10%的电极导线显示出阈值会发生增高或降低的变化,因此在进行序列成像(serial imaging)时应特别注意这一点。
2.4 引起感知功能异常:一方面,导线电极尖端的感应电流可导致过感知引起高频率起搏,或导致感知不足引起起搏抑制。另一方面,电磁场干扰可能会造成CIED误感知——误认作心房或心室的高频率起搏事件,或则引起起搏器产生致命性起搏抑制,或则在追踪模式下出现快速心室起搏,抑或在ICD患者中导致不适当电击。
2.5 诱发恶性心律失常:除了由静磁场引起的不可预知的起搏模式转换产生竞争心律外,射频磁场和梯度磁场还会诱导产生感应电流,当其足够大时,其亦可夺获心肌而引起意外起搏,也同样能产生竞争心律,引起致死性室性心动过速或心室颤动(图2);此外,磁场中电极的热效应也可刺激心肌而诱发心律失常。
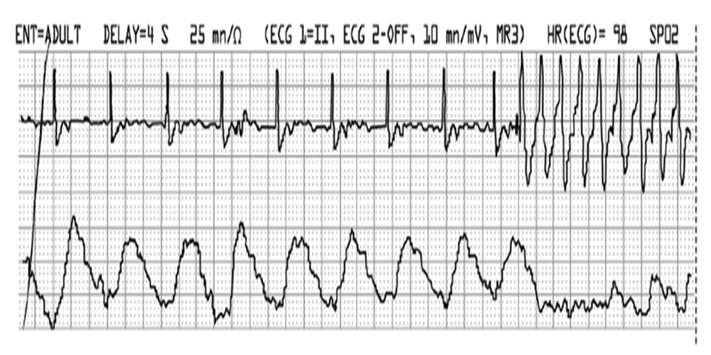
图2 诱发电流夺获心肌所引起的室性心动过速(Medtronic公司提供)[12]。
2.6 起搏器电池损耗:MRI检查时,射频磁场和梯度磁场可造成起搏器短暂性电流输出增加,进而损耗电量。
2.7 电源开启重置(power-on-reset):是指电子设备通电或重新启动后,相关电学参数恢复成缺省(或默认)状态的过程。在电池损耗或电磁场干扰的情况下,CIED的参数便可能被错误的重置,这通常是三种磁场复杂作用的结果。
2.8 CIED对MRI成像的影响:研究显示,CIED可降低MRI成像的准确性[6]。在MRI检查时,铁磁性或非铁磁性金属可干扰静磁场和梯度磁场的均匀性,产生磁敏感性伪影(图3),影响周围15 cm内人体区域的MRI影像,其中铁磁性金属的影响程度更大。CIED造成的伪影常比实物大,可能影响疾病的诊断[13],尤以对右心室和左心室前壁的影响最为明显[14]。
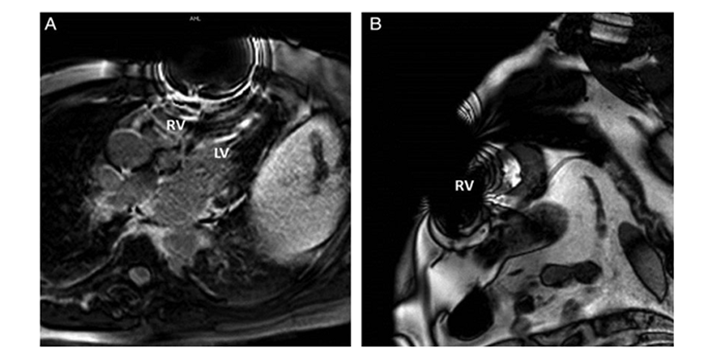
图3. CIED患者左胸典型的MRI伪影图像[14]。A. 四腔切面;B. 短轴切面。RV, 右心室; LV, 左心室
3 MRI兼容性CIED技术上的改进
自2008年Medtronic公司推出SureScan起搏系统以来,许多起搏器制造商也相继进行了技术改造,生产出新一代的MRI兼容性起搏器。这些技术改进主要集中于以下几个方面[15, 16]:(1)尽量减少系统内铁磁性金属的含量,以降低CIED在磁场内的作用力,同时减少MRI检查时的磁敏感性伪影;(2)调整起搏器开关:由于Hal传感器在磁场环境中能有效调控开关,故用Hal传感器代替簧片开关;(3)防止电磁干扰:屏蔽内部电路,有效防止磁场的干扰;(4)设置专用于MRI检查的起搏和感知模式,在MRI检查时启动,在检查结束时,该模式恢复正常,从而有效防止电源开启重置;(5)电极导线的系统改造:一是改变导线构造和内部设计,如使用钢丝纤维导线,改变扭转斜度和导线尺寸等;二是在导线连接处使用滤波电容,减少交变磁场导致的导线电极升温效应,最大程度地减少电极顶端的能量释放。
表1 CIED在MRI检查时的安全等级[17, 18]

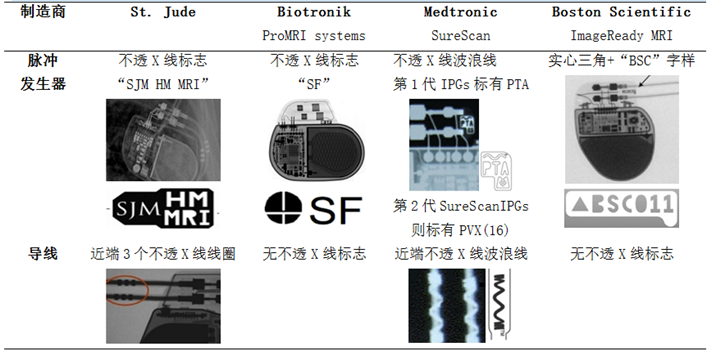
然而,尽管作了上述修改,但不同厂家生产的起搏器的铁磁性成份和内部电路尚不统一,因此应重视其各自在MRI环境中的特定使用条件。美国FDA使用“MRI安全”,“MRI条件性安全”和“MRI不安全”等专业性术语来标注CIED在接受MRI检查时的安全性(表1)。需要强调的是,目前没有标示“完全MRI安全(completely MRI safe)”的CIED,每款MRI兼容性CIED均有特定的使用条件,只有在符合这些条件下应用才不会造成特殊风险,也不会损害MRI的图像质量[12](表2)。此外,不同厂家的脉冲发生器和电极导线相互并不兼容,故在起搏器更换前应予以确认;如不能得到相关资料,尚可通过简单X线胸片以查看各制造商的特征性标识(表3)。鉴于上述原因,MRI兼容性CIED也被广泛称作MRI条件性CIED(MRI conditional CIED)。
表2 植入MRI兼容性(条件性)起搏器患者接受MRI检查的要求[19]

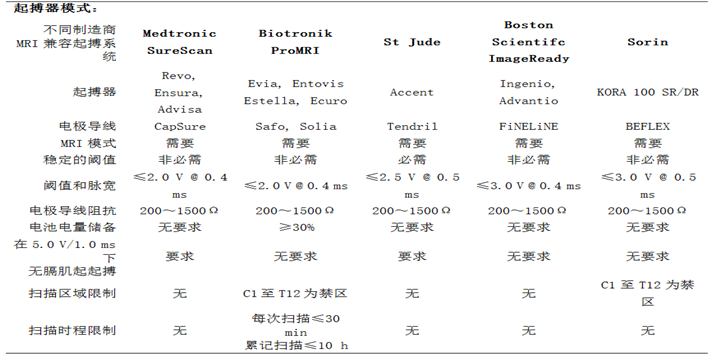 注: ①SAR, specifc absorption rate, 特殊吸收辐射率;②相比之下,Medtronic公司SureScan起搏系统接受MRI检查的兼容性好,其上市也最早,并有较多临床数据。
注: ①SAR, specifc absorption rate, 特殊吸收辐射率;②相比之下,Medtronic公司SureScan起搏系统接受MRI检查的兼容性好,其上市也最早,并有较多临床数据。
表3 不同制造商MRI兼容性(条件性)起搏器的标识[12, 16]
4 MRI兼容性CIED的临床应用
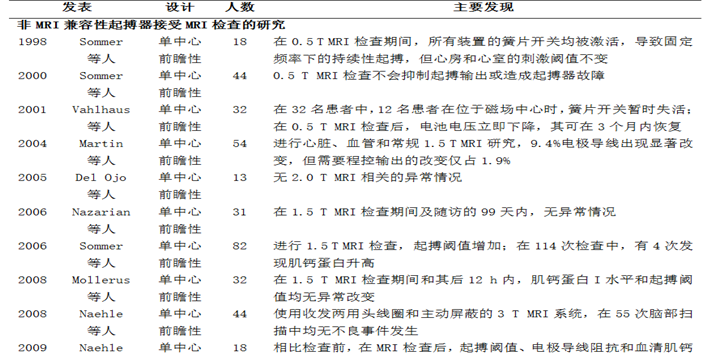
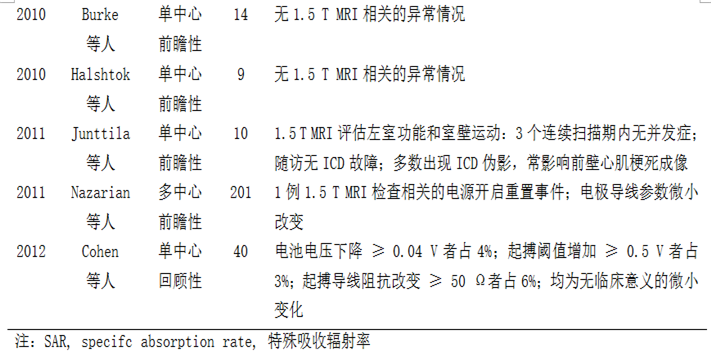
除了技术上的革新,研究者也在临床实践中逐步探索CIED患者接受MRI检查的安全性条件(表4):从早期非MRI兼容性起搏器到MRI兼容性起搏器,再到MRI兼容性ICD,近20年来,人们积累了大量的临床数据。
表4 CIED临床研究的沿革[20]



注:SAR, specifc absorption rate, 特殊吸收辐射率
直到2008年,Medtronic公司生产的EnRhythm MRI SureScan起搏系统才在欧洲上市,这是最早运用于临床的MRI兼容性起搏系统,由EnRhythmMRI脉冲发生器和CapSureFix 5086 MRI电极导线组成。Wilkoff等[21]进行了一项前瞻性非盲法随机对照临床研究,464名患者植入了EnRhythm MRI SureScan起搏系统,随机分成实验组(n = 258)和对照组(n = 206),实验组于术后9~12周行MRI检查,扫描范围限于避开胸部,仅检查第1颈椎以上和第12胸椎以下区域。结果在MRI检查期间和检查后,未出现MRI相关的并发症(持续性室性心律失常、起搏抑制和电源开启重置等);起搏阈值和感知幅度(sensed electrogram amplitude)的变化极小,且两组相似,证明了EnRhythm MRI SureScan起搏系统在1.5 T条件化MRI检查中的安全性。目前,我国已经较普遍地临床应用Medtronic等公司的MRI兼容性起搏系统。
Wollmann等[22]观察了36名植入EnRhythm/Advisa MRI SureScan起搏系统的患者(平均年龄69 ± 13岁;50%是高度AVB),在1.5 T下接受心脏MRI检查的安全性。结果在MRI检查期间、检查后即刻、检查后第3个月和第15个月,均无MRI相关不良事件发生;与基线相比,心室感知和起搏阻抗改变[感知:基线值9.8 ± 5.3 mV,检查后即刻值10.3 ± 5.3 mV,P< 0.05;系统阻抗(输出5V):基线值508 ± 75Ω;检查中值516 ± 47Ω;检查后15个月值482 ± 58Ω,P < 0.05];起搏阈值(脉宽0.4ms)不变(基线值0.84 ± 0.27 V;检查中值0.82 ± 0.27 V;检查后即刻0.84 ± 0.24 V;检查后3个月0.85 ± 0.23 V;检查后15个月0.90 ± 0.67 V)。上述结果表明,植入EnRhythm/Advisa MRI SureScan起搏系统的患者接受心脏MRI检查是安全的,但可能伴随有不影响临床治疗安全的参数变化。
德国Biotronik公司生产的ProMRI系统是全球种类最全的MRI兼容性起搏系统,其脉冲发生器有Evia、Estella和Effecta三种类型,导线则有Solia、Safio、Siello、Setrox和Selox五种类型。Wollmann等[23]为评估该起搏系统在MRI环境下的可行性,进行了一项单中心前瞻性非随机的研究,31名患者植入Evia SR-T/DR-T起搏器和Safio S导线,在1.5T下接受脑部和低位腰椎的MRI检查。结果是,在随访的3个月内未发生MRI相关的严重不良事件;检查后1个月,电极导线参数与基线相比无差别,包括心房/心室感知基线值3.2±2.1/15.0±6.0 mV,检查后1月值3.2±2.1/14.9±6.5 mV;心房/心室起搏阈值(脉宽0.4 ms)基线值0.68±0.18 V /0.78±0.22 V,检查后1月值0.71±0.24 V /0.78±0.22 V(P = ns);由于起搏器的存在,使脑部弥散加权序列成像出现伪影,但不影响其它序列(如FLAIR)。因此,植入Evia起搏器的患者在预设条件进行MRI检查是安全可行的。然而,在临床实践中,若植入MRI兼容性CIED的患者行MRI检查,仍存在受法律和传统习惯等因素限制的问题。正在进行的Really ProMRI注册研究[24],将评估真实临床实践中MRI兼容性CIED患者每年MRI的检查率和检查的受限因素。
目前,CIED患者仍只限于接受1.5 T以下的MRI检查,3.0 T MRI检查尚存在安全隐患。Gimbel等[25]报道了16例CIED患者接受3.0 T MRI检查的试验,其中9例起搏器患者,6例ICD患者和1例植入式循环记录器(implantable loop recorder)。结果显示无心律失常出现,同时程控参数、起搏阈值、感知、阻抗和电池参数等均无变化;但有1例患者在检查期间出现胸部烧灼感。随后Gimbel又报道了2例患者在3.0 T MRI检查期间出现了起搏抑制。第1例患者因起搏依赖而在受检前程控为非同步模式,但检查期间却发现,在1次心脏停搏后起搏器被重置为VVI模式,这是一例典型的电磁干扰诱导的输出抑制[26]。第2例患者既往植入ICD,但因潜在窦性心动过缓,而将ICD治疗模式转型为AAI起搏治疗(70 ppm)。当患者进入MRI检查孔后,在射频能量和梯度磁场使用前便出现了起搏抑制,原因是出现了磁流体动力学效应——MRI 诱导主动脉根部血液内带电离子往复运动形成感应电流,进而产生了起搏抑制。患者因有稳定的逸搏心律而安全完成了检查[27]。
5 小结
新一代MRI兼容性CIED的问世,使该患者群从“MRI不安全”向“MR条件性安全”迈出重要的一步,为依赖MRI进行诊断的患者带来了福音。对于65岁以上CIED的候选者,若其既往有MRI检查史,或合并脑卒中、肿瘤和骨关节病等疾病或高危因素,则应考虑植入MRI兼容性CIED;而在MRI检查时,则需要临床医师、影像医师和专业技术人员的共同配合,在相关特定条件和严密监护下进行检查,通常可以在磁场环境中使用脉搏血氧监护仪进行血氧饱和度和心率的监测[12],以策患者安全。
然而,MRI兼容性起搏技术尚处于起步阶段,其长期安全性有待更大规模临床研究的进一步验证,尤其是ICD[28]。此外,目前的安全性结论均来自于1.5 T以下的MRI检查结果,通常可满足绝大部分患者临床需求。而随着3.0 T MRI(信噪比高于1.5 T)的广泛应用,其在成像质量、成像速度、频谱诊断和水成像等特殊显像的优势也日渐突出,可获得更好的心血管、骨关节和脑功能成像。如何解决这一新形势下的挑战,这将成为未来MRI兼容性CIED在技术层面和临床研究方面探索的又一方向。
参考文献
[1] Scholtz L, Sarkin A, Lockhat Z. Current clinical applications of cardiovascular magnetic resonance imaging[J]. Cardiovasc J Afr,2014,25(4):185-190.
[2] Chow G V, Nazarian S. MRI for patients with cardiac implantable electrical devices[J]. Cardiol Clin,2014,32(2):299-304.
[3] Gimbel J R, Johnson D, Levine P A, et al. Safe performance of magnetic resonance imaging on five patients with permanent cardiac pacemakers[J]. Pacing Clin Electrophysiol,1996,19(6):913-919.
[4] Sommer T, Vahlhaus C, Lauck G, et al. MR imaging and cardiac pacemakers: in-vitro evaluation and in-vivo studies in 51 patients at 0.5 T[J]. Radiology,2000,215(3):869-879.
[5] Martin E T, Coman J A, Shellock F G, et al. Magnetic resonance imaging and cardiac pacemaker safety at 1.5-Tesla[J]. J Am Coll Cardiol,2004,43(7):1315-1324.
[6] Levine G N, Gomes A S, Arai A E, et al. Safety of magnetic resonance imaging in patients with cardiovascular devices: an American Heart Association scientific statement from the Committee on Diagnostic and Interventional Cardiac Catheterization, Council on Clinical Cardiology, and the Council on Cardiovascular Radiology and Intervention: endorsed by the American College of Cardiology Foundation, the North American Society for Cardiac Imaging, and the Society for Cardiovascular Magnetic Resonance[J]. Circulation,2007,116(24):2878-2891.
[7] Gotte M J, Russel I K, de Roest G J, et al. Magnetic resonance imaging, pacemakers and implantable cardioverter-defibrillators: current situation and clinical perspective[J]. Neth Heart J,2010,18(1):31-37.
[8] Nazarian S, Beinart R, Halperin H R. Magnetic resonance imaging and implantable devices[J]. Circ Arrhythm Electrophysiol,2013,6(2):419-428.
[9] Bovenschulte H, Schluter-Brust K, Liebig T, et al. MRI in patients with pacemakers: overview and procedural management[J]. Dtsch Arztebl Int,2012,109(15):270-275.
[10] Luechinger R, Duru F, Scheidegger M B, et al. Force and torque effects of a 1.5-Tesla MRI scanner on cardiac pacemakers and ICDs[J]. Pacing Clin Electrophysiol,2001,24(2):199-205.
[11] Luechinger R, Duru F, Zeijlemaker V A, et al. Pacemaker reed switch behavior in 0.5, 1.5, and 3.0 Tesla magnetic resonance imaging units: are reed switches always closed in strong magnetic fields?[J]. Pacing Clin Electrophysiol,2002,25(10):1419-1423.
[12] Ahmed F Z, Morris G M, Allen S, et al. Not all pacemakers are created equal: MRI conditional pacemaker and lead technology[J]. J Cardiovasc Electrophysiol,2013,24(9):1059-1065.
[13] Roguin A, Zviman M M, Meininger G R, et al. Modern pacemaker and implantable cardioverter/defibrillator systems can be magnetic resonance imaging safe: in vitro and in vivo assessment of safety and function at 1.5 T[J]. Circulation,2004,110(5):475-482.
[14] Nordbeck P, Ertl G, Ritter O. Magnetic resonance imaging safety in pacemaker and implantable cardioverter defibrillator patients: how far have we come?[J]. Eur Heart J,2015.
[15] Jung W, Zvereva V, Hajredini B, et al. Safe magnetic resonance image scanning of the pacemaker patient: current technologies and future directions[J]. Europace,2012,14(5):631-637.
[16] van der Graaf A W, Bhagirath P, Gotte M J. MRI and cardiac implantable electronic devices; current status and required safety conditions[J]. Neth Heart J,2014,22(6):269-276.
[17] Hundley W G, Bluemke D A, Finn J P, et al. ACCF/ACR/AHA/NASCI/SCMR 2010 expert consensus document on cardiovascular magnetic resonance: a report of the American College of Cardiology Foundation Task Force on Expert Consensus Documents[J]. J Am Coll Cardiol,2010,55(23):2614-2662.
[18] Cronin E M, Wilkoff B L. Magnetic resonance imaging conditional pacemakers: rationale, development and future directions[J]. Indian Pacing Electrophysiol J,2012,12(5):204-212.
[19] Ferreira A M, Costa F, Tralhao A, et al. MRI-conditional pacemakers: current perspectives[J]. Med Devices (Auckl),2014,7:115-124.
[20] Jung W, Jackle S, Zvereva V. MRI and implantable cardiac electronic devices[J]. Curr Opin Cardiol,2015,30(1):65-73.
[21] Wilkoff B L, Bello D, Taborsky M, et al. Magnetic resonance imaging in patients with a pacemaker system designed for the magnetic resonance environment[J]. Heart Rhythm,2011,8(1):65-73.
[22] Wollmann C G, Thudt K, Kaiser B, et al. Safe performance of magnetic resonance of the heart in patients with magnetic resonance conditional pacemaker systems: the safety issue of the ESTIMATE study[J]. J Cardiovasc Magn Reson,2014,16:30.
[23] Wollmann C G, Steiner E, Vock P, et al. Monocenter feasibility study of the MRI compatibility of the Evia pacemaker in combination with Safio S pacemaker lead[J]. J Cardiovasc Magn Reson,2012,14:67.
[24] Maglia G, Curnis A, Brieda M, et al. Assessing access to MRI of patients with magnetic resonance-conditional pacemaker and implantable cardioverter defibrillator systems: the Really ProMRI study design[J]. J Cardiovasc Med (Hagerstown),2014.
[25] Gimbel J R. Magnetic resonance imaging of implantable cardiac rhythm devices at 3.0 tesla[J]. Pacing Clin Electrophysiol,2008,31(7):795-801.
[26] Gimbel J R. Unexpected asystole during 3T magnetic resonance imaging of a pacemaker-dependent patient with a 'modern' pacemaker[J]. Europace,2009,11(9):1241-1242.
[27] Gimbel J R. Unexpected pacing inhibition upon exposure to the 3T static magnetic field prior to imaging acquisition: what is the mechanism?[J]. Heart Rhythm,2011,8(6):944-945.
[28] Kodali S, Baher A, Shah D. Safety of MRIs in patients with pacemakers and defibrillators[J]. Methodist Debakey Cardiovasc J,2013,9(3):137-141.